Đảm bảo cung ứng thuốc phòng, chống dịch Covid-19
Bộ Y tế đã ban hành quyết định số 3416/QĐ-BYT về hướng dẫn chẩn đoán và điều trị Covid-19 do chủng virus Corona mới (Sars - CoV-2) thay thế “Hướng dẫn chẩn đoán và điều trị Covid-19 do chủng vi rút Corona mới (SARS-CoV-2)” ban hành kèm theo Quyết định số 2008/QĐBYT ngày 26/4/2021 của Bộ trưởng Bộ Y tế.
Trong đó, tại mục 6 các biện pháp điều trị khác có nêu một số thuốc mới được đưa vào hướng dẫn: Thuốc chứa hoạt chất Enoxaparin, thuốc chứa hoạt chất Tocilizumab và thuốc Regen-Cov2 (kháng thể đơn dòng kép gồm casirivimab 600mg và Imdevimab 600mg). Đây là các thuốc hiếm về nguồn cung, ít hoặc không có giấy đăng ký lưu hành tại Việt Nam.
Để đảm bảo cung ứng đủ thuốc và kịp thời phục vụ nhu cầu phòng, chống dịch bệnh, Cục Quản lý dược đề nghị các cơ sở sản xuất, nhập khẩu thuốc tiếp tục tăng cường nguồn cung ứng các thuốc nêu trên, chủ động liên hệ với các cơ sở khám bệnh, chữa bệnh để kịp thời nắm bắt nhu cầu thuốc để cung ứng cho các cơ sở khám chữa bệnh. Cục Quản lý dược sẽ thêm mới các hoạt chất trên lên hệ thống báo cáo tồn thuốc Covid-19 (https://duocquocgia.com.vn), yêu cầu các cơ sở sản xuất, nhập khẩu thuốc thực hiện cập nhật đầy đủ thông tin tồn thuốc, nguyên liệu làm thuốc trên hệ thống trực tuyến này.
Thông tin về thuốc chứa Enoxaparin
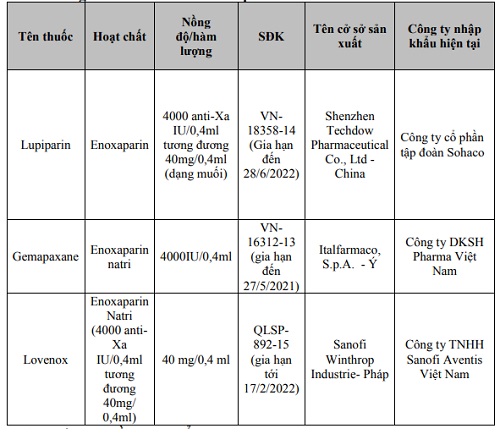 |
Thông tin về kháng thể đơn dòng: Công ty TNHH Roche Pharma (Việt Nam) thông tin về việc công ty đang tiến hành các nghiên cứu lâm sàng về hiệu quả và an toàn của 2 loại thuốc Ronapreve (gồm bộ đôi hai kháng thể đơn dòng Casirivimab và Imdevimab) và Tocilizumab (Actemra) trong điều trị Covid-19 và cam kết hỗ trợ ưu tiên đảm bảo cung ứng đủ thuốc điều trị cho Việt Nam (nếu có nhu cầu)./.
Văn Nam
Dành cho bạn
Đọc thêm


Ngày 27/3: Giá cà phê đảo chiều giảm, hồ tiêu ổn định

Ngày 27/3: Giá lúa gạo tại Đồng bằng sông Cửu Long biến động

Ngày 27/3: Giá bạc trong nước và thế giới nối dài đà giảm

Ngày 27/3: Giá heo hơi tại miền Nam tăng, miền Bắc tiếp tục giảm

Chủ động kịch bản ứng phó xung đột Trung Đông, giữ vững chuỗi xuất khẩu nông sản

Đẩy nhanh lộ trình xăng sinh học E10
































